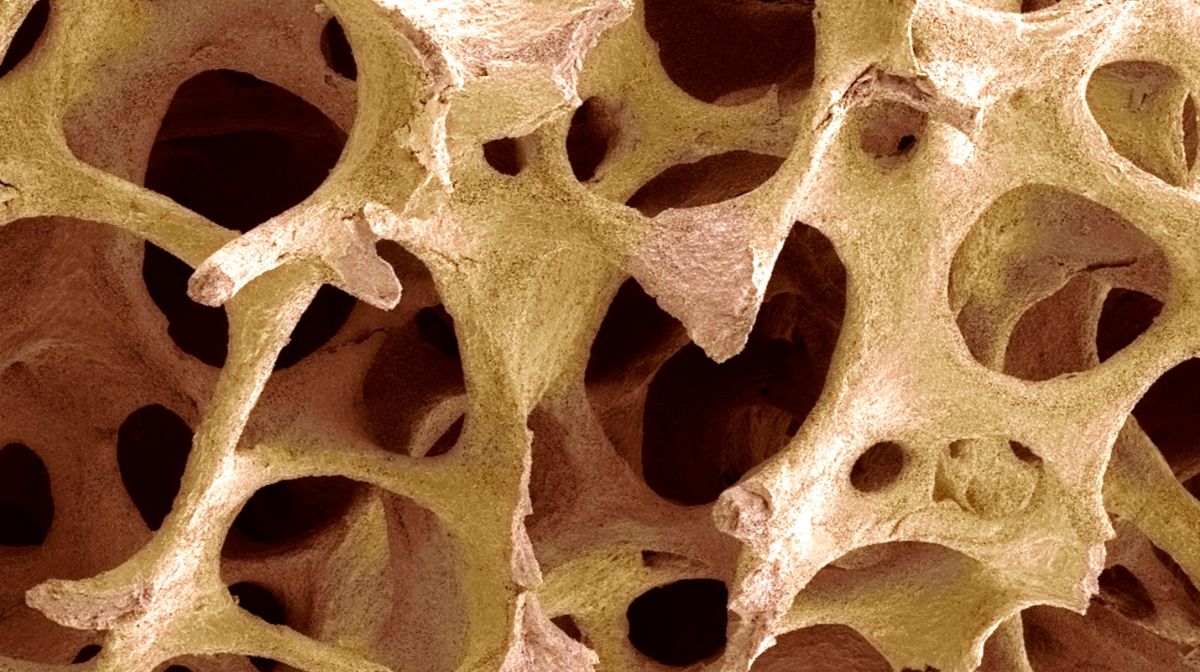
En caso de fractura, al menos tres poblaciones de células madre participan en la reconstrucción ósea, provenientes de la médula ósea, el periostio y los músculos esqueléticos. Un equipo de investigadores acaba de demostrar que si estas poblaciones tienen características moleculares muy variadas cuando están “en reposo”, al menos dos de ellas emprenden un programa común y coordinado en cuanto aparece una lesión ósea.
El daño óseo da como resultado la activación inmediata de un mecanismo de reparación tisular. En el Instituto Mondor de Investigaciones Biomédicas1, El grupo de Céline Colnot, especializado en biología del aparato locomotor, ha demostrado recientemente que al menos tres poblaciones de células madre participan en este proceso: las de la médula ósea, anidadas en el corazón del hueso, las de la membrana externa del hueso (periostio), pero también los presentes en los músculos esqueléticos adyacentes al hueso lesionado.
Para comprender mejor la participación de estas diferentes poblaciones de células, el equipo las estudió en ratones, antes y después de una fractura. Inicialmente, se llevaron a cabo experimentos in vitro y vivir describir las características asociadas a la proliferación de los tres tipos de células madre, su capacidad de migración y su diferenciación. Este trabajo demostró que estas células tienen un destino diferente dependiendo de su origen. Los derivados de la médula ósea difieren sólo en osteoblastos, las células que forman la matriz ósea. Los que se encuentran en el periostio, a su vez, tienen el mayor potencial para la regeneración ósea: de hecho, pueden diferenciarse en osteoblastos, pero también en condrocitos, las células que forman el cartílago. Finalmente, las células madre musculares dan lugar preferentemente a los condrocitos.
Luego, los investigadores estudiaron el perfil de expresión génica de las células madre musculares y periósticas, las más efectivas en el proceso de reparación ósea. Estos análisis transcriptómicos, realizados a escala de células individuales (célula a célula), se realizaron en colaboración con el equipo de Mickaël Ménager de la Universidad de París.dos. El objetivo de los investigadores era poder identificar las vías moleculares activadas en cada célula en un momento dado.
permitir, fibrosisdiferenciación
En ausencia de daño óseo, los científicos observaron una gran heterogeneidad entre las distintas poblaciones celulares estudiadas (e incluso dentro de cada una de ellas), con una importante diversidad en los marcadores moleculares que expresan. Pero esta variedad desaparece en el caso de una lesión a reparar: tres días después de una fractura, todas las células activan vías moleculares similares, en particular una vía ya conocida por su papel en la formación de hueso llamada BMP (por Proteína morfogenética ósea). Como evidencia, la inactivación del receptor BMPR1A involucrado en esta vía conduce a un retraso en la reparación ósea, y las células madre del periostio y el músculo esquelético muestran un defecto en la activación y diferenciación. ” Este estudio nos permite comprender mejor el proceso de reparación ósea. Descubrimos que las células madre en reposo aparentemente muy variadas tienen la capacidad de entrar en acción cuando están dañadas, activando las mismas vías moleculares. También descubrimos la existencia de una etapa intermedia, con un estado fibrogénico de las células madre que parece preceder a su diferenciación en células óseas funcionales. “, dice Céline Colnot. Además del aspecto fundamental, estos resultados ayudan a comprender las anomalías en la reparación ósea que se observan en algunas personas. ” En la neurofibromatosis tipo 1, por ejemplo, los pacientes presentan fracturas que no cicatrizan, con formación de fibrosis permanente a nivel del periostio. Esto ahora puede explicarse por un defecto en la activación de las células madre que les impide pasar de la etapa fibrogénica a la de células diferenciadas. Hemos identificado la vía BMP como involucrada en esta transición, pero aún quedan por descubrir otras vías. Nuestro trabajo unicelular debería permitirnos describir más “, prevé Céline Colnot
Calificaciones :
1 : unidad 955 Inserm/UPEC, IMRB, equipo Biología del sistema neuromuscularCréteil
dos : unidad 1163 Inserm/Universidad de París, equipo Respuestas inflamatorias y redes transcriptómicas en enfermedades y director de LabTech Single-Cell@Imagine
Fuente : Julián et al. Las células madre/progenitoras esqueléticas en el periostio y el músculo esquelético comparten una respuesta molecular común a la lesión ósea. J Bone Miner Res, edición en línea 2 de junio de 2022. DOI: 10.1002/jbmr.4616
Lee también

“Propensa a ataques de apatía. Evangelista de la cerveza. Café incurable. Experto en Internet”.